La próxima gran revolución médica podría no ocurrir en un quirófano, sino en nuestras propias venas. Desde hace décadas, la medicina está luchado contra un desafío fundamental: cómo atacar enfermedades sistémicas, como el cáncer, sin dañar al paciente en el proceso. Tratamientos potentes como la quimioterapia operan bajo una estrategia de «tierra quemada»; son un bombardeo de área que, si bien afecta a los tumores, también devasta células sanas de rápido crecimiento, causando efectos secundarios debilitantes. Esta crudeza no selectiva ha sido el estándar, pero representa una frontera que la ciencia busca desesperadamente superar.

Microrrobot magnético, diseñado para cirugía ocular, sobre la yema de un dedo para mostrar su escala. Fuente: ‘Microrobots: 21st century eye surgeons’ (Portland Press, 2020) / ETH Zürich. Licencia: CC BY 4.0.
Una de las respuestas a este dilema podría estar emergiendo de la convergencia de dos campos tecnológicos exponenciales. Por un lado, la nanorrobótica, que podría darnos la capacidad de diseñar y construir máquinas microscópicas capaces de navegar por el torrente sanguíneo. Por otro lado, la inteligencia artificial, que actuará como el «cerebro» o la «torre de control» externa. Esta sinergia no es ciencia ficción lejana; es la base sobra la que se trabaja para diseñar una futura generación de terapias de precisión: flotas de nanobots guiadas por IA, programadas para cazar células cancerosas una por una o administrar fármacos con una precisión hasta ahora no conseguida.
El cuerpo del nanobot
Para operar dentro del cuerpo humano, un «cirujano nanobótico» debe ser diminuto, biocompatible y, sobre todo, móvil. La escala de estos dispositivos va desde unos pocos micrómetros (millonésimas de metro) hasta nanómetros (milmillonésimas), miles de veces más pequeños que el grosor de un cabello humano.
Su construcción es una proeza de la nanoingeniería, utilizando diversos materiales:
- Origami de ADN: Una de las técnicas más elegantes, que aprovecha la capacidad natural del ADN para plegarse. Los científicos diseñan hebras de ADN sintético que se autoensamblan en formas 3D predeterminadas (como cajas o barriles) que podrían transportar una carga útil.
- Enfoques Bio-híbridos: En lugar de construir desde cero, esta técnica trata de cooptar la maquinaria de la naturaleza, por ejemplo, uniendo nanopartículas terapéuticas a bacterias como la E. coli, que usan sus flagelos naturales como motor.
- Materiales Sintéticos y Biodegradables: Se exploran polímeros, hidrogeles e incluso aleaciones metálicas (como magnesio-zinc) diseñadas para corroerse y disolverse de forma segura en el cuerpo una vez completada su misión.
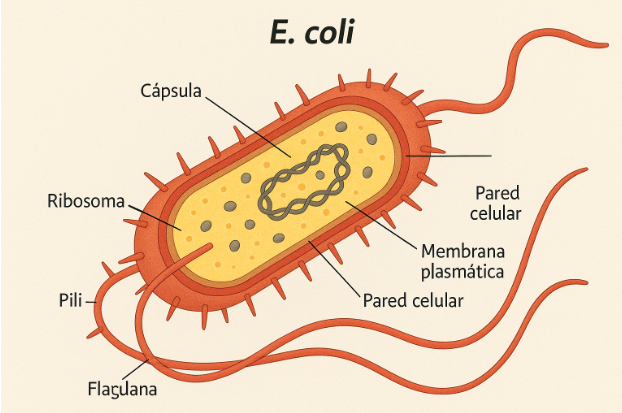
Diagrama de la estructura de la bacteria E. coli.
Un nanobot estático es inútil. Su propulsión se logra principalmente de dos maneras: autopropulsión (química), como los nanomotores que usan la enzima ureasa para descomponer la urea (abundante en la vejiga) como combustible; o, el método más controlado, la propulsión por campos externos. Aquí, los nanobots con un componente magnético son dirigidos con precisión por bobinas electromagnéticas fuera del cuerpo, permitiendo una teleoperación no invasiva.
El cerebro de la IA piloto
Un nanobot, por muy sofisticado que sea, es solo el «cuerpo»; necesita un «cerebro» que lo guíe. Debido a las limitaciones de escala, este cerebro no reside en el robot, sino fuera del paciente, en un potente sistema informático que fusiona la inteligencia artificial con la imagenología médica en tiempo real. Esta es la «torre de control» externa que permite la navegación de precisión.
El sistema opera en un bucle de control en tiempo real:
Ver, pensar y actuar:
- Ver (Imagen): Técnicas como la Imagen por Resonancia Magnética (IRM) o el ultrasonido proporcionan un mapa 3D en vivo del interior del cuerpo. Estas imágenes permiten localizar tanto la anatomía del paciente (un tumor, un coágulo) como la flota de nanobots.
- Pensar (IA): El flujo de imágenes alimenta a los algoritmos de IA. Modelos de machine learning identifican el objetivo y calculan la trayectoria óptima para llegar a él. Algoritmos más avanzados, como el aprendizaje por refuerzo profundo (Deep Reinforcement Learning), pueden entrenar al «piloto» de IA para navegar por entornos complejos y dinámicos como el flujo sanguíneo, aprendiendo a «nadar» contra la corriente o aprovecharla.
- Actuar (Campos Magnéticos): La trayectoria calculada por la IA se traduce en comandos precisos para el sistema de propulsión, por ejemplo, ajustando las bobinas electromagnéticas miles de veces por segundo para guiar a los nanobots magnéticos por la ruta planificada.
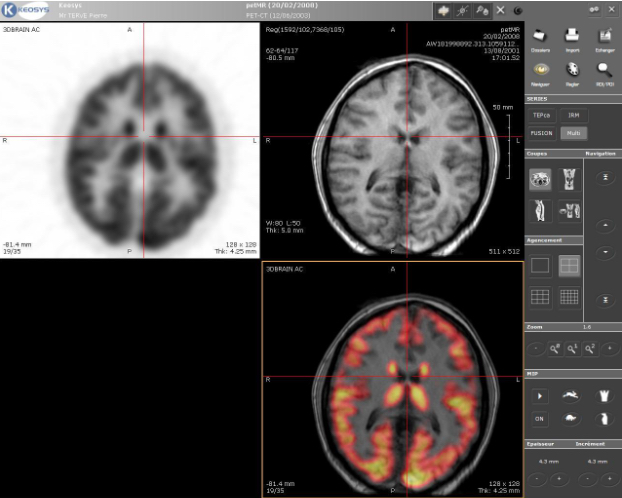
Escáner PET-MRI cerebral fusionado, destacando regiones de alta actividad metabólica (en rojo y amarillo) By Mco44 – Own work, Public Domain, https://commons.wikimedia.org/w/index.php?curid=3587922
La IA también permite la inteligencia de enjambre (Swarm Intelligence), coordinando el comportamiento colectivo de millones de nanobots para que actúen como una «cuña» coordinada para penetrar un coágulo o rodear un tumor.
Misiones de alta precisión
Esta tecnología no es solo una especulación lejana; se está demostrando su viabilidad en investigaciones preclínicas avanzadas y en el probable futuro desarrollo comercial.
- Oncología (Cortar Suministros): Una de las estrategias más innovadoras, desarrollada por la Universidad Estatal de Arizona, utiliza nanobots de origami de ADN. Estos nanobots transportan la enzima trombina (un potente coagulante). Están diseñados para buscar una proteína (nucleolina) que solo se encuentra en los vasos sanguíneos que alimentan tumores. Al encontrarla, el nanobot se abre y libera la trombina, creando coágulos localizados que cortan el suministro de sangre y «matan de hambre» al tumor. En modelos animales, esta técnica provocó una rápida necrosis tumoral.
- Oncología (Activación Inmune): La startup española Nanobots Therapeutics desarrolla nanobots autopropulsados por ureasa (el combustible químico). Su misión es navegar por la vejiga para penetrar tumores. Su carga útil no es quimioterapia, sino una molécula que «desenmascara» el tumor , convirtiendo un tumor «frío» (invisible al sistema inmune) en uno «caliente», provocando un ataque inmunitario localizado. En modelos preclínicos, lograron una reducción del 90% del tumor con una sola dosis.
- Neurología (Cruzar Barreras): El cerebro es increíblemente difícil de tratar debido a la barrera hematoencefálica. La empresa estadounidense Bionautlabs está desarrollando «Bionauts», microrobots guiados magnéticamente para navegar por el tejido cerebral. Su trabajo ya ha recibido designaciones de la FDA: «Fármaco Huérfano» para un Bionaut que entrega quimioterapia directamente en gliomas (tumores cerebrales) y «Dispositivo de Uso Humanitario» para tratar el Síndrome de Dandy-Walker (un trastorno neurológico) realizando microcirugía para perforar un quiste cerebral sin cirugía abierta.

Imagen referencia de la startup española Nanobots Therapeutics. Acceso a su web: https://www.nanobotstx.com/
El ecosistema y los desafíos monumentales
El potencial de la nanorrobótica médica con toda probabilidad impulsará un ecosistema comercial emergente. Empresas como Bionautlabs y Nanobots Therapeutics están a la vanguardia, y las proyecciones de mercado estiman un crecimiento de miles de millones de euros para la próxima década, impulsado por las aplicaciones en oncología y neurología.
Sin embargo, el camino desde el laboratorio hasta la clínica está plagado de desafíos monumentales. El primero es técnico y biológico: ¿cómo se fabrican miles de millones de estos robots de grado clínico de forma rentable? ¿Cómo se asegura que el sistema inmunitario no los identifique y destruya como invasores extraños? Y, ¿qué pasa con ellos al final de su misión? La posibilidad de «bio-nanopolución» (acumulación de nanomateriales no degradables en el cuerpo) es una preocupación seria que exige materiales biodegradables.
El segundo desafío es regulatorio y ético. Un nanobot guiado por IA no es un fármaco ni un dispositivo médico convencional; es un híbrido complejo. Agencias como la FDA y la EMA deben crear nuevos marcos de aprobación. Esto conduce a la pregunta legal y ética fundamental: si un enjambre de nanobots guiado por una IA comete un error y daña tejido sano, ¿quién es el responsable? ¿El médico, la empresa de software de IA o el fabricante del robot?
Una revolución en gesta
La imagen de cirujanos nanobóticos navegando por nuestras venas ya no pertenece exclusivamente al reino de la ciencia ficción. Los componentes fundamentales de esta visión —nanoestructuras programables como el origami de ADN y sistemas de guiado por inteligencia artificial — ya se vislumbran como una realidad tangible en laboratorios y startups de todo el mundo. La convergencia de la nanotecnología, la robótica y la IA ha abierto una de las fronteras más prometedoras de la medicina moderna.
El camino hacia la aplicación clínica rutinaria será largo y los desafíos, tanto técnicos como éticos, son formidables. El progreso deberá ir de la mano de un desarrollo igualmente riguroso de nuevos marcos regulatorios y un debate social sobre el control y la responsabilidad. Sin embargo, el potencial para transformar fundamentalmente la medicina es innegable. Estamos asistiendo al inicio de una transición para dejar atrás las intervenciones sistémicas de «tierra quemada» y avanzar hacia cirugías celulares de precisión. La revolución no ocurrirá de la noche a la mañana, pero se está gestando, prometiendo un futuro en el que las enfermedades más devastadoras podrían ser curadas desde dentro, casi célula a célula.


